我,是誰?(完整版) mitochondrial donation (3-Person IVF) & Germline Modification
(口述:吳庶忠教授 │香港科技大學生命科學部客座教授)
生殖科技的發展日漸成熟,引伸的倫理議題大都離不開生命的抉擇、借精、代孕母等。然而,今天更值得關注的生殖科技議題是三人體外受孕的研究(mitochondrial donation)。自2008年起,英國的HFEA (Human Fertilisation and Embryology Authority) 有權制訂相關的規則以容許進行有關避免嚴重線粒體疾病的技術,2014年2月英國政府就相關的規定進行諮詢,2014年6月當局發表一份關於透過進行Pronuclear transfer (PNT)[1]或Maternal Spindle Transfer (MST)[2]而減少線粒體疾病(mitochondrial disease)的遺傳的科研回顧報告[3]。若議會通過草案,英國便可合法地進行有關線粒體捐贈(mitochondrial donation),驟聽似乎是醫學界及生殖科技界上的一大突破,然而當中存在著更大的倫理爭議及危機。
人體的「電池」─ 線粒體
線粒體(mitochondria)是人體細胞內的細小組織(ORGANELLE),是唯一擁有自己的DNA (即mtDNA)的細小組織。線粒體是用以提供能量維繫身體各器官的正常運作。當線粒體出現故障(malfunction)便會引致身體器官出現嚴重疾病,故障的主因是線粒體所包含的DNA出現變異,或細胞核中會影響線粒體所需的基因產物(gene products, 即RNA / protein)的DNA出現變異,最後引致細胞所能產生的能量出現問題,影響器官的正常運作。如線粒體中的DNA (mtDNA)出現變異,會引致嚴重的遺傳性疾病,有機會降低嬰孩的生存率,引致長期病患、身體痛楚、衰弱等,而線粒體捐贈的研究是為了減少或避免此類因mtDNA變異而引發的嚴重的疾病遺傳到下一代。
線粒體捐贈 = 醫治嚴重遺傳性疾病的喜訊?
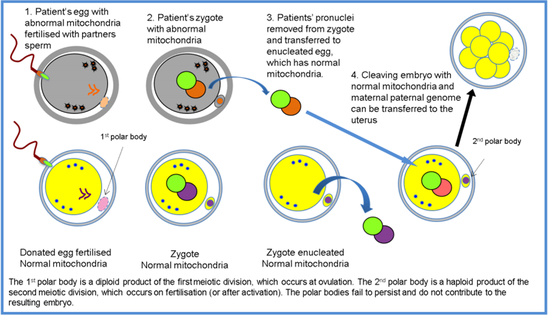
現行的胚胎植入前的遺傳診斷(Preimplantation genetic diagnosis, PGD),能診斷因細胞核的DNA出現變異而引致的疾病,而PGD的限制是不能應用於變異原因不明的情況,因而HEFA於2010年便就線粒體捐贈(Mitochondrial Donation)而進行科研,線粒體捐贈或稱3-person IVF,顧名思義指牽涉整個體外受孕(In Vitro Fertilization,IVF)的過程的人數不止2個人,而是最少有3個人。而最基本的3人組合可以是:親生父、母、及卵子捐贈者。當中所牽涉的科技包括:PNT及MST (圖1 & 2),簡單而言,MST就是透過顯微技術,把生母A的卵母細胞(oocyte)中的核遺傳物質(nuclear genetic material)抽出移至捐贈者B已移除核遺傳細胞的卵母細胞中;而PNT同樣利用相類的顯微技術,把已受精的卵母細胞中的母及父系原系(maternal- and paternal-derived pronuclei)的核遺傳物質抽出,移至由捐贈者的卵母細胞及父系精子結合而成的已去核的合子(enucleated donor zygote)中,二者最大的分別是MST在卵子未受精前進行,PNT則在卵子受精後細胞進行分裂前進行,如此便可減低因親生母親的卵母細胞的線粒體變異而引致的遺傳疾病傳給下一代及後代。
圖1:Maternal Spindle Transfer (MST) (圖片來源:MRC Harwell, https://www.har.mrc.ac.uk/news-events/news-archive/mitochondrial-replacement-not-unsafe)
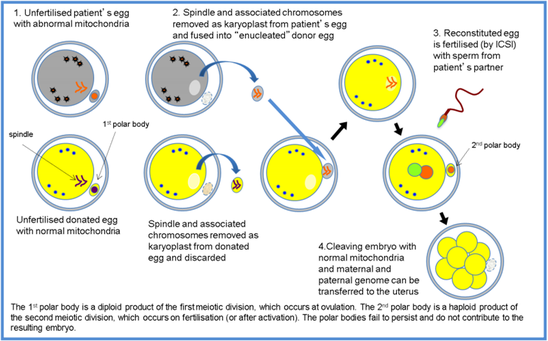
圖2:Pronuclear Transfer (PNT)(圖片來源:MRC Harwell, https://www.har.mrc.ac.uk/news-events/news-archive/mitochondrial-replacement-not-unsafe)
嬰兒,是誰和誰和誰…的下一代?
撇除艱深的專有名詞不看,我們都不難發現不論是MST還是PNT的技術,都存在著極大的爭議,不能避免要思考的是當中的科技應用所牽涉的道德倫理議題,包括:
一、透過這種方法而誕生的孩子擁有最少3人的基因;
MST或PNT的關鍵是在於第三者所捐贈的卵子,而捐贈者的卵子的mtDNA不帶有任何的變異。即使科研報告表示過程中會把捐贈者的卵母細胞中的核遺傳物質抽走,然而亦無人能確定當中的準確度及成功率;再者捐贈者的卵母細胞的線粒體中DNA仍然存在,因而科學家亦不能否認被「修改」的卵母細胞同時存在著兩位女性的DNA。更複雜的是PNT需要以體外受孕的方法製造最少兩組合子,一組是擬定的原生父母的精子及卵子、另一組是擬定的父親的精子及捐贈的卵子,而再透過科技把兩組合子中的核遺傳物質修改,就如MST的情況,合子的DNA組合必然同時包含擬定的原生父母及卵子捐贈者的DNA,如此,這項科技所帶來的問題就是一個嬰孩本應只能擁有父及母(不論是親生的還是透過配子捐贈)的DNA,然而現在卻最少擁有3人(親生父母或配子捐贈者,以及卵子捐贈者)的DNA。
二、 可透過進行修改人類的遺傳基因而引致生殖細胞系(germline)改變;
支持提倡線粒體捐贈的科技的人聲稱此項技術令生殖細胞系改變的風險很低,原因是mtDNA只佔人體大約20,000基因組中的37條基因;但其實已有研究證實這些基因會影響人的老化的過程甚至延長人的壽數。透過線粒體捐贈而產生的胚胎及後代,是構成與進行生殖細胞系的基因工程的一個過程[4]。由於有關基因的科研及技術應用一直都存在著很大的分歧,即使對基因改造的食物,人都會小心奕奕地處理,並求有清楚的說明及標籤,難道要研究基因科研的技術在人類的應用上不應更加小心嗎?歐洲的生物倫理委員會(Committee on Bioethics,DH-BIO)所編制的人權公約和生物醫學(Convention on Human Rights and Biomedicine)中清楚表明禁止有關修改人類生殖細胞系的活動。[5]因為一旦線粒體捐贈成功通過應用在人類上,人類的生殖細胞系嚴格來說最終便會被修改,會為人類的歷史及演進帶來翻天覆地並不可逆轉的改變。
生殖細胞的修改與複製人(Human cloning)的情況相似,這些基因工程同樣會對人類的身份與尊嚴構成威脅;早在1997年,聯合國教育、科學與文化組織(UNESCO)在第29屆全體會議中通過的《世界人類基因組與人權宣言》(Universal Declaration on the Human Genome and Human Rights)第11條聲明:違背人的尊嚴的一些做法,如用複製技術繁殖人的做法,是不允許的。要求各國和各有關國際組織進行合作,以便根據本《宣言》所陳述的原則,鑑別這些做法,並在國家或國際一級採取各種必要的措施。[6]
科技是否已成熟並確定不會對使用者或嬰兒造成不可逆轉或不可修補的錯誤或傷害等等,並未有定論,外國的科研專家表示此類抽取替換線粒體的基因的實驗只是在動物身上進行初步的嘗試,即使在靈長類的動物中都未曾進行相類似的實試,[7]這些技術根本是在人類歷史中史無前例的嘗試,而當中最危險的是一旦生殖細胞系改變,就會造成長期、永久、甚至不可逆轉的傷害,[8]但不論是MST或PNT都牽涉生殖細胞系的改變,未全面考慮當中的安全性或準確性便謬然立法推行, 實在不智。我們現正經歷重要的分水嶺,雖然「造成不可逆轉的傷害」看似是滑坡的道德論證,然而當沒有人能夠證明生殖細胞系的改變是安全的,我們便不能否定當中的可能存在的危害性。
因此,以立法的形式容許這項科研應用在人類以前,應有更多的研究結果以論證mtDNA的「移植」的好處及影響,而科研的對象更應該與人類的狀況及結構相近,如靈長類動物,而不是單單在低等的哺乳類動物身上。在未有具體可靠的科研結果前,是否應考慮延長立法諮詢的時間,而不是硬堆此高風險的科學研究技術?誠然,醫療科技的安全是很值得關注的範疇,即使已有在動物身上所進行的科研報告,我們仍然關注是否再進一步需有相關的臨床醫學研究報告,以致當考慮是否立法准許線粒體捐贈的科研技術應用在醫療層面上時,能有更可靠的研究結果證明此項科技的安全性及可應用性。
三、更改生殖細胞系非必需,可考慮其他代替技術;
今天已有相對成熟的科技在不用更改生殖細胞系的情況下處理有關線粒體基因變異所引致的疾病,例如病毒載體(viral vectors ),簡單來說就是將基因物質(genetic material)傳送至相關細胞中,[9]在處理線粒體變異所引致的遺傳病的情況上,可透過分子生物科的技術把健康的線粒體取代有缺陷的線粒體基因,而這項體細胞基因修改(somatic gene modification)的技術所帶來的危害性遠比生殖細胞系修改(germline modification)少。因此,英國下議院在考慮是否立法推行線粒體捐贈以外,可考慮其他相對更安全的代替技術以作醫療用途。
至於科技以外的道德倫理議題亦不能忽視,很多涉及生殖科技的道德爭議,如:生命的定義與價值、涉及第三者捐贈配子,誰才是父母、嬰兒是否有權知道捐贈者的真正身份等早已出現。而個人的價值與尊嚴,優生的問題更是爭論不休。
一、 個人的價值與尊嚴?[10]
基因科研的成果,大大刺激了「選擇」、優生的實行。康德曾就人的尊嚴作出論述,認為人之所以有尊嚴是因為人有理性,自主性,能為自己設定價值目標,當因著基因科技而出現優生的情況,則人的基因配置便由父母、醫生甚至國家所決定,個人僅是設計者所選擇、決定和製造的結果,對人的自主性並尊嚴構成嚴重的威脅,令人「那種作為自己生命的完整主人的權利,便被粗暴地踐踏了。」達特茅斯學院(Dartmouth College)的生物倫理學家Ronald Green亦提到透過線粒體捐贈而出生的孩子,長大後對於自己的身份(identity)會有疑問,到底「我是誰?」、「我和其他人一樣只有兩個父母嗎?」 、「還是我只是一個被研發的新的被造物(new type of creature)?」[11]
另外,中國社會中對尊嚴的理解或許會有所不同,未必會把個人的自主性當作是尊嚴的核心內涵,然而中國古代思想家亦提倡人比萬物尊貴是因為人有道德。事實上,「人類基因改造對人類平等尊嚴的踐踏只是個次要的錯誤,最根本的錯誤則是僭取上帝或自然的權力的錯誤。人類掌握了具有巨大破壞力的技術,卻沒有正確使用技術的道德和智慧。」[12]
二、優生與墮胎?
線粒體捐贈/ 更改胚胎的染色體組會提高後代被破壞的機會,這類「更正」(“revisionist”)的優生學概念其實源自選擇論("selectionist")[13],正如在美國曾向罪犯、精神病患者、智障人士、某些種族或社經地位低的人實施的強制性絕育及20世紀歐洲的納粹黨屠殺的情況。至於優生與墮胎的倫理爭議是另外一個複雜的議題,需用更多的篇章解釋,在此不詳敍,可參考其他相關文章。
三、金錢與權力-社會階層的不公義?
科研往往所需花費的時間與金錢都不是可以簡單計算,因而將科研成果應用在不同層面的生活範疇時,可想而知並不是每個人都可以負擔。如果線粒體捐贈的科研目的是為了減少嚴重的遺傳性疾病,對於未能承擔龐大醫療開支,但又面對此情況的女性、或夫婦來說,豈不只是告訴他們可存有一個遙不可及的盼望?如此推說,只有富人才有機會能「醫治」線粒體變異所引致的嚴重遺傳性疾病,這會是變相的「優生」或「選擇論」嗎?豈不更拉遠社會不同階層人士的距離?不論在健康、財富、甚或接受教育、工作等等的機會上,令貧者愈貧、富者愈富嗎?
線粒體捐贈,迄今未知它在人類身上實行的安全性,亦存在極多的倫理爭議,是否必然要國家以制度推行這樣的政策,實需從長計議,不該貿然通過。
[1] PNT:Technique to transfer a couple’s nuclear genetic material from a fertilised egg (zygote) into an donor zygote with its nuclear genetic material removed
[2] MST:Technique to transfer the nuclear genetic material from a woman’s egg into a donated egg with its nuclear genetic material removed
[3] “Third scientific review of the safety and efficacy of methods to avoid mitochondrial disease through assisted conception: 2014 update “,http://www.hfea.gov.uk/docs/Third_Mitochondrial_replacement_scientific_review.pdf
[4] “The British Embryo Authority and the Chamber of Eugenics”,Nov 2013,
http://www.huffingtonpost.com/stuart-a-newman/mitochondrial-replacement-ethics_b_2837818.html
[5] “ Convention for the Protection of Human Rights and Dignity of the Human Being with regard to the Application of Biology and Medicine: Convention on Human Rights and Biomedicine”,1997,http://conventions.coe.int/Treaty/en/Treaties/Html/164.htm
[6] “Universal Declaration on the Human Genome and Human Rights”,UNESCO,http://portal.unesco.org/en/ev.php-URL_ID=13177&URL_DO=DO_TOPIC&URL_SECTION=201.html
[7] “A slippery slope to human germline modification”,July 2013,http://www.nature.com/news/a-slippery-slope-to-human-germline-modification-1.13358
[8] “Brave New Cells ?”,Dec 2012,http://www.project-syndicate.org/commentary/the-risks-of-mitochondrial-research-in-the-uk-by-donna-dickenson
[9] “Working with viral vectors”,2013,Stanford University,http://web.stanford.edu/dept/EHS/prod/researchlab/bio/docs/Working_with_Viral_Vectors.pdf
[10] Lu F. “Genetic Technology and Human Dignity.” In J. Chan(editor). 2007. “Bioethics in the Context of Chinese Societies.” International Journal of Chinese & Comparative Philosophy of Medicine. Vol. 5, 1, 73-85.
[11] “Proposed Treatment To Fix Genetic Diseases Raises Ethical Issues”,Oct 2013,http://www.npr.org/blogs/health/2013/10/09/229167219/proposed-treatment-to-fix-genetic-diseases-raising-ethics-issues
[12] 同10。
[13] A. Wagner. “Evolution: Selectionist View.” In D.N. Cooper(editor). 2003. “Encyclopedia of the Human Genome.” Vol. 2.

